日前,北京商报今日记者获悉,乐普生物抗PD—1抗体普妥珠单抗注射液上市申请已获批,这是乐普生物首个商业化产品,也是国内第八个PD—1抗体产品但目前国内PD—1单克隆抗体市场竞争趋于激烈在拓展海外市场方面,百济神州,君实生物,信达生物的PD—1单克隆抗体相继受挫后来者乐普生物的PD—1单克隆抗体有多少机会
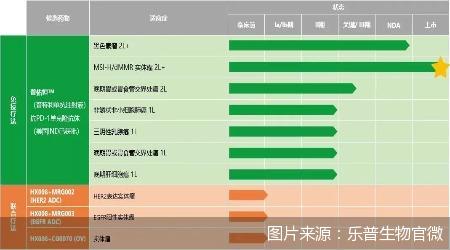
对于乐普生物来说,普妥珠单抗注射液是其首个商业化产品乐普生物作为乐普系,是从乐普医疗分拆出来的日前,乐普生物正式登陆港交所上市此前,由于公司没有产品上市,乐普生物持续亏损2020年,乐普生物净亏损从2019年的5.16亿元增长19%至6.13亿元,两年净亏损超过10亿元
乐普生物的普珠单抗注射液作为首个商业化产品,面临着相当大的竞争伴随着普妥昔单抗注射液的获批,国内已批准上市的PD—1单克隆抗体产品增至8个,其余包括君实生物的Territuximab,信达生物,恒瑞医药的Karelizumab,百济神州的Tirelizumab,康方生物的Pai Ampley单克隆抗体,宇恒制药的Sepali单克隆抗体,傅宏Hanlinsrulizumab
医保谈判后,PD—1单克隆抗体利润被挤出,年治疗费用降至5万元/年君实生物是R&D首家国产PD—1抗体药物制造商2021年财报显示,君实生物PD—1 Trepril单克隆抗体实现营收4.12亿元,同比下降58.96%,较2020年的10.03亿元减少近6亿元
君生物将Tereplizumab营收下滑归因于进入医保后降价60%以上,以及PD—1产品在国内市场的商业竞争日益激烈。
要抢占国内市场份额,乐普生物的PD—1单克隆抗体产品势必面临降价的选择业内人士表示,乐普生物的PD—1单克隆抗体产品想要进入医保,定价只能低于目前进入医保的价格
鉴于公司的差异化竞争优势,乐普生物相关负责人今日向北京商报记者表示,对比所有已上市或进入三期临床试验的抗PD—1抗体,普妥珠单抗注射液的平均半衰期分别为21.8天和38.2天此外,延长的半衰期不会导致额外的不良事件,其临床疗效极佳
拓展出海市场也是目前各企业的应对策略之一在国际化发展方面,乐普生物加大力度拓展国际市场,推动全球新药联合开发,合作和授权2022年1月,美国美国食品药品监督管理局批准了用普特利珠单抗治疗晚期实体瘤的新药临床试验申请
不过,第一批进入者已经传出出海受阻的消息,乐普生物能否成功进入海外市场还有待时间检验2021年3月,君实生物向FDA提交了PD—1单克隆抗体产品的上市申请2022年5月,FDA表示,由于与新冠肺炎疫情相关的旅行限制,待完成的现场验证受阻,因此初步上市申请被暂时搁置此外,今年3月,信达生物核心产品Cindilizumab申请上市未获FDA批准,首战告负另有市场消息称,在收到FDA反馈后,诺华并未提交合作方百济神州PD—1替利珠单抗二线治疗非小细胞肺癌的上市许可申请
声明:以上内容为本网站转自其它媒体,相关信息仅为传递更多企业信息之目的,不代表本网观点,亦不代表本网站赞同其观点或证实其内容的真实性。投资有风险,需谨慎。
 三大航货运业务逆势增长,燃油附加费翻番 三大航去年亏损仍在加剧,航空业出路何在。3月30日晚间,国内三大航司相继发布2021年年报,三大航营收均录得增...
三大航货运业务逆势增长,燃油附加费翻番 三大航去年亏损仍在加剧,航空业出路何在。3月30日晚间,国内三大航司相继发布2021年年报,三大航营收均录得增...  3999元起,小米11Ultra手机限时特惠150 日前,小米春季发布会上正式推出了小米11Ultra,该机拥有黑白两色,精密陶瓷工艺机身,黑色沉稳大气,白色优雅...
3999元起,小米11Ultra手机限时特惠150 日前,小米春季发布会上正式推出了小米11Ultra,该机拥有黑白两色,精密陶瓷工艺机身,黑色沉稳大气,白色优雅...  新北洋:累计回购605万股占比0.9088% 每经AI快讯,新北洋3月31日晚间发布公告称,截至2022年3月31日,公司累计通过回购专用证券账户以集中竞价...
新北洋:累计回购605万股占比0.9088% 每经AI快讯,新北洋3月31日晚间发布公告称,截至2022年3月31日,公司累计通过回购专用证券账户以集中竞价...  中青旅:2021年营收同比增长两成持续布局“旅游+ 中青旅3月31日披露2021年报,公司全年实现营业收入86.35亿元,较上年增加20.76%,实现归属于上市公...
中青旅:2021年营收同比增长两成持续布局“旅游+ 中青旅3月31日披露2021年报,公司全年实现营业收入86.35亿元,较上年增加20.76%,实现归属于上市公...  高值设计·重构未来——SK瓷砖x金堂奖战略合作云发 SKCERAMICS2022随着消费新升级,新生代消费群体对居住空间的诉求,越来越艺术化、多元化、个性化。SK...
高值设计·重构未来——SK瓷砖x金堂奖战略合作云发 SKCERAMICS2022随着消费新升级,新生代消费群体对居住空间的诉求,越来越艺术化、多元化、个性化。SK...  605389长龄液压3月24日收盘小幅上涨0.57 2022年3月24日长龄液压(605389)收盘点评:长龄液压今日小幅上涨.57%,早盘低开-0.50%,报4...
605389长龄液压3月24日收盘小幅上涨0.57 2022年3月24日长龄液压(605389)收盘点评:长龄液压今日小幅上涨.57%,早盘低开-0.50%,报4...  600358国旅联合3月24日全天上涨2.48%, 2022年3月24日国旅联合(600358)收盘点评:国旅联合今日上涨2.48%,早盘低开-0.41%,报7....
600358国旅联合3月24日全天上涨2.48%, 2022年3月24日国旅联合(600358)收盘点评:国旅联合今日上涨2.48%,早盘低开-0.41%,报7....  600386北巴传媒3月24日收盘数据:较昨日下跌 2022年3月24日北巴传媒(600386)收盘点评:北巴传媒今日微跌-.25%,早盘高开0.25%,报4.0...
600386北巴传媒3月24日收盘数据:较昨日下跌 2022年3月24日北巴传媒(600386)收盘点评:北巴传媒今日微跌-.25%,早盘高开0.25%,报4.0...  海能实业:2021年度独立董事述职报告王义华 安福县海能实业股份有限公司2021年度独立董事述职报告王义华各位股东及股东代表:本人作为安福县海能实业股份有限...
海能实业:2021年度独立董事述职报告王义华 安福县海能实业股份有限公司2021年度独立董事述职报告王义华各位股东及股东代表:本人作为安福县海能实业股份有限...  601598中国外运3月24日股价收盘3.88元与 2022年3月24日中国外运(601598)收盘点评:中国外运今日股价与昨日持平早盘高开0.77%,报3.91...
601598中国外运3月24日股价收盘3.88元与 2022年3月24日中国外运(601598)收盘点评:中国外运今日股价与昨日持平早盘高开0.77%,报3.91... 
 601138工业富联3月24 2022年3月24日工业富联(60113...
601138工业富联3月24 2022年3月24日工业富联(60113...  陈小春开启京东汽车超级直播夜 11月9日晚18点,京东汽车11.11超...
陈小春开启京东汽车超级直播夜 11月9日晚18点,京东汽车11.11超...  挑战善行者丨2021速8酒店 热爱不止,善行不息善行者是一种勇气善行者...
挑战善行者丨2021速8酒店 热爱不止,善行不息善行者是一种勇气善行者...  布局宠物蓝海市场安心养宠物计 京东健康宠物医院作为安心养宠物最重要的升...
布局宠物蓝海市场安心养宠物计 京东健康宠物医院作为安心养宠物最重要的升... 

 苏炳添用9秒83的佳绩带领亚 每0.01秒的提升都是汗水与泪水...
苏炳添用9秒83的佳绩带领亚 每0.01秒的提升都是汗水与泪水...  4×100米接力决赛 中国男 4×100米接力·决赛中国女队4...
4×100米接力决赛 中国男 4×100米接力·决赛中国女队4...  JBL/UA PROJECT 在这七月热汗运动季,由高保真至潮...
JBL/UA PROJECT 在这七月热汗运动季,由高保真至潮...  中国队“00后”纷纷登上东京 杨倩、管晨辰、李雯雯、全红婵……...
中国队“00后”纷纷登上东京 杨倩、管晨辰、李雯雯、全红婵……...  体育赛事招商的三大注意事项 今年4月姚明和篮协对CBA商务开发权的争...
体育赛事招商的三大注意事项 今年4月姚明和篮协对CBA商务开发权的争...  传统体育文化的两大现代价值 中国传统体育文化丰富多彩,内容博大精深,...
传统体育文化的两大现代价值 中国传统体育文化丰富多彩,内容博大精深,...  当今世界体育对人的价值体现在 不知你想过没有,在当今这个高度互联网化、...
当今世界体育对人的价值体现在 不知你想过没有,在当今这个高度互联网化、...  体育分析中机器学习的标准:预 运动分析有相当一部分属于机器学习,即从数...
体育分析中机器学习的标准:预 运动分析有相当一部分属于机器学习,即从数...  进行冬奥会体育营销的五个关键 明年冬奥会将在北京和张家口举行,关于奥运...
进行冬奥会体育营销的五个关键 明年冬奥会将在北京和张家口举行,关于奥运...  父母如何从家庭教育当中反思自 某天晚上睡不着,忽然想到能够写这么一个角...
父母如何从家庭教育当中反思自 某天晚上睡不着,忽然想到能够写这么一个角...  思维教育对幼儿的四大好处 思想教育对幼儿的益处,幼儿思想处于直观行...
思维教育对幼儿的四大好处 思想教育对幼儿的益处,幼儿思想处于直观行...  父母教育孩子前必须要知道的前 网上的很多文章提到过,一些懵懂型鸡娃的家...
父母教育孩子前必须要知道的前 网上的很多文章提到过,一些懵懂型鸡娃的家...  华为是第一大客户EDA第一股 在半导体芯片设计领域,EDA软件也是卡脖...
华为是第一大客户EDA第一股 在半导体芯片设计领域,EDA软件也是卡脖...  新的设计和技术风向奥迪gra 2021年9月3日消息,奥迪将在2021...
新的设计和技术风向奥迪gra 2021年9月3日消息,奥迪将在2021...